Очень часто можно услышать мнение, что атом будучи составной частью молекулы, обладает теми же свойствами и имеет аналогичную структуру. Такая позиция лишь отчасти имеет право на существование, поскольку частицы имеют общие и отличительные признаки. Для начала достаточно рассмотреть свойства двух объектов, и на их основе делать дальнейшие выводы.
Атом
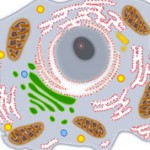
Атом можно рассматривать как элементарную частицу однородного вещества. Такое вещество, по определению, состоит только из одного химического элемента (С, N, O и другие с периодической таблицы Менделеева). Именно наименьшая часть таких элементов, которая может быть носителем их свойств, и называется атомом. Согласно последним современным представлениям, атом состоит из трех составляющих: протонов, нейтронов и электронов.
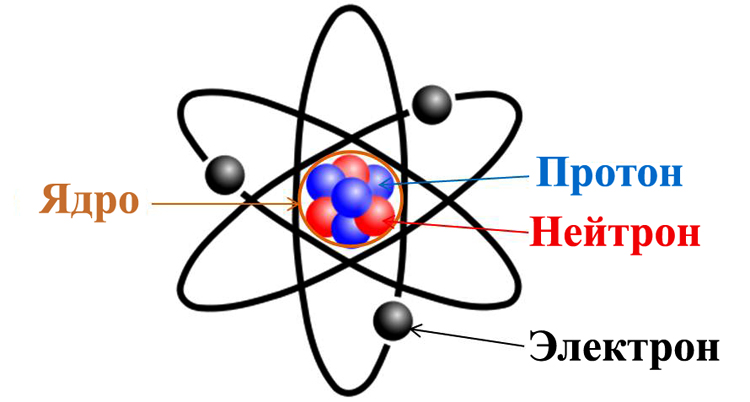
Атом
Первые две субчастицы вместе составляют базовое ядро, которое имеет положительный заряд. Двигающиеся вокруг ядра электроны привносят компенсационный заряд с противоположным знаком. Таким образом, делается первый вывод, что большинство атомов — электрически нейтральны. Что касается оставшейся части, то в силу различных физико-химических процессов, атомы могут либо присоединять, либо отпускать электроны, что приводит к появлению заряда. Атом имеет массу и размер (определяется размерами ядра) и определяет химические свойства вещества.
Молекула
Молекула является минимальной структурной единицей вещества. Такое вещество может состоять из нескольких химических элементов. Однако, молекулой можно считать и одноатомное вещество одного химического элемента — инертный газ аргона. Как и атомы, является электрически нейтральной. Ионизировать молекулу можно, но уже значительно сложнее: атомы внутри молекулы связаны между собой ковалентной, либо ионной связью. Поэтому присоединить или забрать электрон становится значительно сложнее. Большинство молекул имеет сложную архитектурную постройку, где каждый атом заранее занимает отведенное ему место.
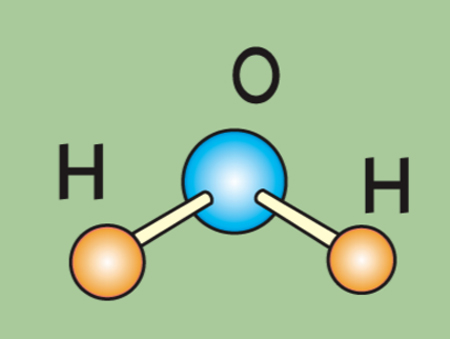
Строение молекулы воды
Атом и молекула: общие свойства
Строение. Обе частицы являются структурными единицами вещества. При этом под атомом подразумевается один определенный элемент, молекула же включает в себя уже несколько химически связанных атомов, но структура (положительное ядро с отрицательными электронами) остается той же.
Электрическая нейтральность. При отсутствии внешних факторов — взаимодействия с другим химическим веществом, направленного электрического поля и других раздражителей, — атомы и молекулы не имеют заряда.
Замещение. Атом может выступать как молекула в одном случае — при работе с инертными газами. Также молекулой может считаться одноатомная ртуть.
Наличие массы. Обе частицы имеют свою четкую массу. В случае атома масса зависит от химического элемента и определяется весом ядра (протон почти в 1500 раз тяжелее электрона, поэтому вес отрицательной частицы часто не берется во внимание). Масса молекулы определяется исходя из ее химической формулы — элементов, входящих в ее состав.
Атом и молекула: отличные свойства
Неделимость. Атом является мельчайшим элементом, из которого нельзя выделить еще меньшую частицу. (Получение иона влияет только на заряд, но не на вес). Молекулу, в свою очередь, можно разделить на более мелкие молекулы или можно разложить на атомы. Процесса распада легко добиться с использованием химических катализаторов. Иногда достаточно просто нагреть вещество.
Свободное существование. Молекула может свободно существовать в природе. Атом существует в вольной форме лишь в двух случаях:
- Как одноатомная ртуть или инертный газ.
- В условиях космоса — как отдельные атомы могут находиться любые химические элементы.
В остальных случаях атом всегда входит в состав молекулы.
Образование заряда. Взаимодействие между ядром и электроном в атоме можно легко преодолеть даже мельчайшим электрическим полем. Таким образом, — из атома легко получить положительный или отрицательный ион. Наличие химических связей между атомами внутри молекулы требует приложения гораздо большего электрического поля или взаимодействия с другим химически активным веществом.